2018.7.19
医家向け自動血圧計および血圧測定モジュールを搭載した医療機器の点検のご案内
この度、当社子会社であるオムロン大連有限公司(以下、大連工場)において製造し日本国内で販売している下記医家向け自動血圧計、血圧測定モジュールおよびこれを搭載した医療機器(以下、対象商品)につき、計量法および特定計量器検定検査規則が定めた検査方法を一部満たさない方法で検査を行い出荷していたことが判明いたしました。
当社では、直ちに経済産業省を始めとする関係機関に報告の上で、対応を検討した結果、対象商品につき点検させていただくことにしましたので、ご案内申し上げます。
なお、対象商品の医療機器としての安全性、有効性については問題がなく、問題発生後、社内での調査および確認をいたしましたが、圧力測定精度に問題は見つかっておりません。
対象商品の点検は、圧力測定精度に問題がないことの確認のための点検となります。
皆様にはご迷惑をおかけすることとなり深くお詫び申し上げます。何卒、ご理解とご協力をお願いいたします。
記
(対象商品)
| 機種名 | 発売時期 | 形態・販売対象 | 出荷台数(累計)※ |
|---|---|---|---|
| 自動血圧計 HBP-9020/9021 |
2009年11月 | 医療機関向け完成品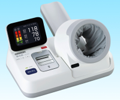 |
HBP-9020:26,202台 HBP-9021:3,785台 |
| 自動血圧計 HBP-1300 |
2013年1月 | 医療機関向け完成品 |
14,300台 |
| 血圧測定モジュール HBP-M3500 |
2008年12月 | 医療機器搭載用部品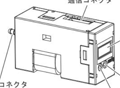 |
162,353台 (内HBP-608EVⅢ搭載分1,081台/ HBP-2070/2071搭載分8,237台) |
| 生体情報モニタ HBP-608EVⅢ (上記M3500を搭載しているため対象) |
2011年8月 (2016年8月生産終了) |
医療機関向け完成品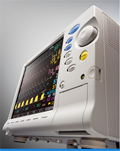 |
|
| 生体情報モニタ HBP-2070/2071 (上記M3500を搭載しているため対象) |
2009年9月 (2070:2017年5月 /2071:2016年5月生産終了) |
医療機関向け完成品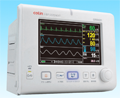 |
※2018年6月15日までに、当社より出荷したもの。
(経緯)
当社では製造工程の管理強化に取り組んでおり、大連工場においても、その一環として確認を行っておりました。本事案は、その中で判明したものです。その後、直ちに、社内にて詳細に確認をおこない、対象商品を特定するとともに、製造、出荷を停止いたしました。
本事案の発生原因は、大連工場において、対象商品の製造手順書に計量法の要求する検査事項の記載が一部漏れていたことによるものです。
対象商品以外の計量法が適用となる当社商品については、その要求する検査事項を満足していることを確認しております。
(対応)
当社といたしましては、対象商品をお使いの納入先様に当社より個別にご連絡の上、点検を実施させていただきます。
なお、この点検は、計量法に基づく特定計量器としての圧力測定精度の確認のために行うものです。
お客様を始め関係各位にご迷惑とご心配をおかけしますことを、重ねて深くお詫び申し上げます。
なお、本件に関するお客様からのお問い合わせは、以下の窓口で応対させていただきます。
お問い合わせ先
- ・ お問い合わせ窓口:オムロン点検受付センター
- ・ 受付時間:午前9時から午後5時(土日、祝日を除く)
- ・ 電話番号:0120-57-5155
- ・ FAX番号:0120-10-1625
- ・ メールアドレス:kenko-web-ohq@omron.com
以上